Σοβαρές αναταράξεις στον χώρο της πλαστικής χειρουργικής επέφεραν οι αποκαλύψεις της Διεθνούς Κοινοπραξίας Ερευνητικών Δημοσιογράφων (ICIJ) για τη βλάβη που προκαλούν παγκοσμίως ιατρικές συσκευές και προϊόντα που δεν έχουν ελεγχθεί σωστά. Οι γαλλικές αρχές διέταξαν την απόσυρση δύο τύπων ενθεμάτων σιλικόνης της εταιρείας Allergan που χρησιμοποιούν εκατομμύρια γυναίκες διεθνώς, τα οποία φέρονται να έχουν συνδεθεί με την πρόκληση μιας μορφής λεμφώματος σε εκατοντάδες περιπτώσεις. Άμεση η απαγόρευση χρήσης τους και στην υπόλοιπη Ευρώπη, καθώς η εταιρεία δεν κατάφερε να εξασφαλίσει την αναγκαία σήμανση ασφαλείας που είναι απαραίτητη για τη χρήση τέτοιου είδους προϊόντων.
του Μηνά Κωνσταντίνου
Η Allergan, ένας από τους μεγαλύτερους κατασκευαστές εμφυτευμάτων στήθους στον κόσμο, αποκλείστηκε από την πώληση δημοφιλών προϊόντων της στην Ευρώπη, μετά από απόφαση της Εθνικής Υπηρεσίας Ασφάλειας των Φαρμάκων και των Προϊόντων Υγείας της Γαλλίας (ANSM). Αιτία, η αυξανόμενη ανησυχία σχετικά με τη σύνδεσή τους με μια σπάνια μορφή καρκίνου, του αναπλαστικού μεγαλοκυτταρικού λεμφώματος σε ασθενείς με ενθέματα μαστών (BIA-ALCL).
Η ANSM προχώρησε στην απόφαση αυτή κατόπιν λεπτομερών ερωτημάτων που κατέθεσαν δημοσιογράφοι στη Γαλλία, που εργάστηκαν για την έρευνα του ICIJ για τα «φονικά εμφυτεύματα» (Implant Files). Η έρευνα, στην οποία συμμετείχαν περισσότεροι από 250 δημοσιογράφοι από όλο τον κόσμο και δημοσιεύτηκε τον Νοέμβριο, περιελάμβανε πλήθος στοιχείων για τις σοβαρές βλάβες που προκαλούν διεθνώς ιατρικές συσκευές και προϊόντα που δεν έχουν ελεγχθεί σωστά.
Συγκεκριμένα, αναφορικά με την υπόθεση της Allergan, πρόκειται για τα ενθέματα σιλικόνης τραχείας επιφανείας, τα οποία καλύπτουν το μεγαλύτερο μέρος (85%) της γαλλικής αγοράς, είναι ευρέως διαδεδομένα και στην υπόλοιπη Ευρώπη, καθώς και στη χώρα μας. Τα συγκεκριμένα εμφυτεύματα στήθους, όπως όλα τα ιατρικά εμφυτεύματα, οφείλουν να φέρουν τη σήμανση CE, ώστε να μπορούν να πωληθούν στις 33 ευρωπαϊκές χώρες. Ωστόσο, όπως ανακοίνωσε η γαλλική ρυθμιστική αρχή ANSM την περασμένη Τρίτη, αλλά και η ίδια η εταιρεία, η Allergan δεν κατάφερε να εξασφαλίσει τη σήμανση για δύο από τα πιο δημοφιλή προϊόντα της, τα Microcell και Biocell, με αποτέλεσμα να αποφασιστεί η απαγόρευση και η απόσυρσή τους.
Μάλιστα, η γαλλική ρυθμιστική αρχή (ANSM) τον Νοέμβριο -υπό το βάρος των αποκαλύψεων της ICIJ- συνιστούσε να χρησιμοποιούνται πλέον εμφυτεύματα στήθους λείας επιφανείας ή άλλης τεχνολογίας τραχείας επιφάνεια, αντί για τα συγκεκριμένα προϊόντα τραχείας επιφάνειας, κάνοντας ειδική αναφορά στη σχέση μεταξύ των προϊόντων αυτών και του εν λόγω τύπου καρκίνου. Όπως αναφέρει ο Guardian, που συμμετείχε στην έρευνα της ICIJ, κατόπιν της απόφασης για την αναστολή της έγκρισης ασφαλείας CE για τα προϊόντα αυτά, τέτοιου είδους εμφυτεύματα δεν μπορούν να κατασκευαστούν ή να πωληθούν στην Ευρώπη, ενώ αυτά που βρίσκονται σε νοσοκομεία, κλινικές, ιατρεία ή άλλες υπηρεσίες υγείας που ενδέχεται να τα έχουν στις αποθήκες τους, οφείλουν να αποσυρθούν.
Αξίζει να σημειωθεί ακόμη πως η γαλλική ρυθμιστική αρχή δήλωσε ότι δεν είχε «εντοπίσει κανέναν άμεσο κίνδυνο για την υγεία των γυναικών που φέρουν τα σχετικά εμφυτεύματα», ενώ στην ανακοίνωσή της δεν γίνεται αναφορά στον κίνδυνο πρόκλησης καρκίνου. Ωστόσο, υπάρχει διεθνώς αυξανόμενη ανησυχία για τη σχέση των επίμαχων εμφυτευμάτων με την πρόκληση του σπάνιου λεμφώματος, με στοιχεία που συλλέχθηκαν από πλαστικούς χειρουργούς να κάνουν λόγο για 615 κρούσματα της νόσου και 16 θανάτους, που συνδέονται με ενθεματα στήθους τέτοιου τύπου.
Ο κίνδυνος πρόκλησης λεμφώματος
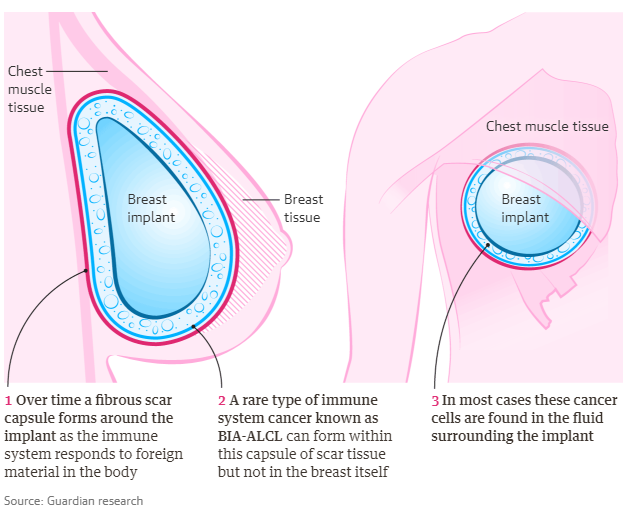
Όπως εξηγούν ιατρικές πηγές με εμπεριστατωμένη γνώση του αντικειμένου στο TPP, κύτταρα του λεμφώματος βρίσκονται στον ουλώδη ιστό και στο αντιδραστικό υγρό γύρω από το ένθεμα, δηλαδή δεν υπάρχουν ή δημιουργούνται από το ένθεμα, αλλά από τον οργανισμό σαν αντίδραση στο ένθεμα. Είναι ένας σπάνιος τύπος λεμφώματος που ανήκει στην κατηγορία των Non-Hodgkin λεμφωμάτων. Σύμφωνα με την ίδια πηγή, η αιτιολογία παραμένει ασαφής, αλλά η πιο επιβεβαιωμένη θεωρία είναι ότι συνδέεται με το λεγόμενο «biofilm».
Το biofilm είναι μια λεπτή στρώση στην επιφάνεια των ενθεμάτων όπου ενσωματώνονται βακτήρια και η οποία περιτυλίγεται από μια προστατευτική στοιβάδα γλυκοπρωτεϊνών. Είναι δύσκολο τεχνικά να αφανιστούν όλα τα βακτήρια κατά τη διαδικασία παρασκευής και έτσι υπάρχει περίπτωση να υπάρχουν σε αδρανή κατάσταση για χρόνια. Η θεωρία υποστηρίζει ότι τα κύτταρα του λεμφώματος μπορεί να προέρχονται από την αντίδραση του οργανισμού στα βακτήρια αυτά στο biofilm που βρίσκεται στο ένθεμα, χωρίς αυτό να έχει αποδειχτεί επιστημονικά. Η γενική 5ετής επιβίωση για ασθενείς με τον συγκεκριμένο τύπο λευκώματος BIA-ALCL (ανεξαρτήτως σταδίου) είναι 89%, πράγμα που σημαίνει πως είναι αντιμετωπίσιμος.
Σύμφωνα με τον Guardian, γυναίκες που έχουν αφαιρέσει τα εμφυτεύματα έχουν καταφέρει να ανακάμψουν πλήρως, αλλά υπογραμμίζεται πως εάν αφεθούν χωρίς θεραπεία, η ασθένεια μπορεί να εξαπλωθεί σε όλο το σώμα, και να απειλήσει ακόμα και τη ζωή τους.
Ακόμη, η βρετανική εφημερίδα φιλοξενεί δηλώσεις της Σούζαν Τέρνερ, επιστήμονα του Πανεπιστημίου του Κέμπριτζ που ερευνά τη σχέση μεταξύ των συγκεκριμένων εμφυτευμάτων τραχείας επιφάνειας και της πρόκλησης του σπάνιου λεμφώματος, η οποία χαιρετίζει την παραπάνω είδηση. Όπως αναφέρει, τα επίμαχα εμφυτεύματα θα πρέπει να αποσυρθούν από την αγορά, μέχρι να γίνουν γνωστά περισσότερα σχετικά με τη σχέση τους με την πρόκληση καρκίνου. Στο ίδιο δημοσίευμα, ο πρόεδρος της Βρετανικής Ένωσης Αισθητικής Πλαστικής Χειρουργικής, Πολ Χάρις, δήλωσε πως η εξέλιξη αυτή θα είναι «αιτία για κατανοητή ανησυχία για πολλούς ασθενείς», συμπληρώνοντας ωστόσο πως «είναι σημαντικό να αναγνωρίσουμε πως αυτό είναι ένα προληπτικό μέτρο».
Σύμφωνα με τα στοιχεία του Διεθνούς Οργανισμού για την Έρευνα για τον Καρκίνο, περίπου 1 εκατ. νέα κρούσματα καρκίνου του μαστού σημειώνονται κάθε χρόνο σε όλο τον κόσμο, με τις γυναίκες να βρίσκονται στο στόχαστρο του συγκεκριμένου καρκίνου κατά 100 φορές πιο συχνά από τους άνδρες. Στην Ευρώπη, μία στις 9 γυναίκες θα νοσήσει από αυτόν κάποια στιγμή στη ζωή της, ενώ για την Ελλάδα, υπολογίζεται πως κάθε χρόνο εμφανίζονται περί τα 6.000 νέα κρούσματα. Συνεπώς, τα νέα στοιχεία που έχουν προκύψει για τους κινδύνους τοποθέτησης των συγκεκριμένων ενθεμάτων, δεν αφορούν μόνο το μέρος εκείνο των γυναικών που προχωρούν σε αισθητικές επεμβάσεις, αλλά και πολλές από εκείνες που βρίσκονται στο στάδιο της αποκατάστασης από τον καρκίνο του μαστού.
Επαγρύπνηση σε Ευρώπη και Αμερική
Αποκαλυπτική για την κατάσταση είναι και η ανακοίνωση της Ευρωπαϊκής Ένωσης Πλαστικών Χειρουργών (EURAPS) προς τα μέλη της, που δεν δόθηκε στη δημοσιότητα αλλά το TPP την έχει στην κατοχή του, που κάνει λόγω ευθαρσώς για τη σύνδεση των ενθεμάτων στήθους τραχείας επιφανείας με το αναπλαστικό μεγαλοκυτταρικό λέμφωμα σε ασθενείς με ενθέματα σιλικόνης (ALCL). Μάλιστα, αναφέρεται σε «περισσότερα από 600 κρούσματα της ασθένειας παγκοσμίως, εκ των οποίων τα 239 στην Ευρώπη, όπου 9 γυναίκες πέθαναν εξαιτίας της ασθένειας».
Σύμφωνα με την ανακοίνωση της EURAPS, οι γυναίκες που φέρουν τα εν λόγω προϊόντα, που χρησιμοποιούνται στις αισθητικές και επανορθωτικές επεμβάσεις μαστού σε μεγάλο μέρος της ευρωπαϊκής αγοράς, δεν αντιμετωπίζουν κάποιον άμεσο κίνδυνο για την υγεία τους. Ωστόσο συμπληρώνει πως «όσες φέρουν σήμερα τα συγκεκριμένα ενθέματα στήθους της Allergan, συνιστάται να παρακολουθούνται συνεχώς από τους ιατρούς τους». Ακόμη, υπογραμμίζεται πως από τις 21 Νοεμβρίου του έτους, ο ANSM έχει συστήσει στους επαγγελματίες υγείας να χρησιμοποιούν κατά προτίμηση τα ενθέματα στήθους με λείο ή άλλης τεχνολογίας περίβλημα, δημόσια σύσταση στην οποία έχει προχωρήσει και η Βρετανική Ένωση Αισθητικής Πλαστικής Χειρουργικής (BAAPS).
Οι Βρετανοί αναφέρουν πως ο κίνδυνος για την υγεία «εμφανίζεται μικρός», συμπληρώνουν ωστόσο πως «είναι κρίσιμο, όλοι οι κίνδυνοι της χρήσης τέτοιων εμφυτευμάτων να έχουν λεπτομερώς συζητηθεί με όλους τους ασθενείς πριν από την επέμβαση, ώστε οι ασθενείς να είναι σε θέση να επιλέξουν όντας ενήμεροι». Αξίζει επίσης να σημειωθεί πως στις συστάσεις της, η Βρετανική Ένωση Αισθητικής Πλαστικής Χειρουργικής (BAAPS) αναφέρει πως «με βάση τα πιο πρόσφατα επιστημονικά στοιχεία που είναι διαθέσιμα, δεν είναι ανάγκη να αφαιρεθούν ή να αλλαχθούν τέτοιου είδους εμφυτεύματα. Πράγματι, η περιττή χειρουργική επέμβαση μπορεί να προκαλέσει πρόσθετη βλάβη σε μικρό αριθμό ασθενών». Ξεκαθαρίζουν ακόμη πως στην περίπτωση που δεν υπάρχει κανένα σύμπτωμα, οι ασθενείς δεν χρειάζεται να κάνουν τίποτα περισσότερο από την τακτική παρακολούθηση από τον ιατρό τους.
Ακόμη, σύμφωνα με την Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA), «τα ενθέματα στήθους, ανεξαρτήτως της υφής της επιφάνειάς τους, συνδέονται με έναν μικρό κίνδυνο» εμφάνισης του εν λόγω τύπου καρκίνου. Οι Αμερικανοί αναφέρουν, σύμφωνα με το NBC News ότι παρακολουθούν τη σχέση μεταξύ των ενθεμάτων στήθους τραχείας επιφανείας και του αναπλαστικού μεγαλοκυτταρικύ λεμφώματος (BIA-ALCL) που σχετίζεται με τα ενθέματα στήθους, ενώ ανακοίνωσαν πως η αμερικανική ρυθμιστική αρχή θα συνεδριάσει τον προσεχή Ιανουάριο, με σκοπό να επανεξετάσει την ασφάλεια όλων των ενθεμάτων στήθους. Αντίστοιχη συνεδρίαση της Προσωρινής Ειδικευμένης Επιστημονικής Επιτροπής (CSST) του ANSM των Γάλλων αναμένεται στις 7-8 Φεβρουαρίου, ώστε να ληφθεί απόφαση σχετικά με τη χρήση των εμφυτευμάτων τραχείας επιφάνειας της εν λόγω εταιρείας.
Υπογραμμίζεται επίσης ότι, σύμφωνα με την FDA, «μπορεί να υπάρχουν πολλοί παράγοντες που εμπλέκονται στην ανάπτυξη του εν λόγω λεμφώματος, όπως τα χαρακτηριστικά του ασθενούς, το ιστορικό της επιχειρησιακής διαδικασίας, τα χαρακτηριστικά του ενθέματος του μαστού -συμπεριλαμβανομένων των επιφανειακών χαρακτηριστικών και της διάρκειας του ενθέματος στήθους».
Παρότι συστάσεις ρυθμιστικών αρχών τρίτων χωρών, τα παραπάνω αποκτούν εξέχουσα σημασία για τη χώρα μας, λαμβάνοντας υπόψη πως οι αντίστοιχες ελληνικές αρχές δεν έχουν προχωρήσει στην παραμικρή επίσημη ανακοίνωση προς το κοινό, σε αντίθεση τις περισσότερες από τις παραπάνω. Σε συνδυασμό με το γεγονός πως τα ελληνικά ΜΜΕ, με προεξέχον το Αθηναϊκό Πρακτορείο και άλλα μεγάλα μέσα ενημέρωσης, αρκέστηκαν στην είδηση πως… απλώς «Ανακαλούνται ενθέματα στήθους επειδή έχασαν τη σήμανση CE» και χωρίς την παραμικρή εξήγηση επί του θέματος, η ενημέρωση γύρω από το ζήτημα κρίνεται επιτακτική και σίγουρα οφείλει να είναι σοβαρότερη.
Σε κάθε περίπτωση, εκείνο που οφείλουν να κάνουν οι ασθενείς που έχουν προχωρήσει σε επεμβάσεις μαστών με ενθέματα ή διατατήρες τραχείας επιφανείας είναι να απευθυνθούν στους ιατρούς τους για την καλύτερη ενημέρωσή τους.
Η θέση της εταιρείας
Την ίδια ώρα, σε ανακοίνωσή της η εταιρεία Allergan υποστηρίζει πως η σήμανση CE για τα συγκεκριμένα προϊόντα της έχει ανασταλεί επειδή «δεν έχει ολοκληρωθεί η συνήθης αναθεώρηση και ανανέωση του φακέλου μας» και υπογραμμίζει πως συνεργάζεται με τις γαλλικές ρυθμιστικές αρχές για τον καθορισμό των κατάλληλων επόμενων βημάτων.
Όπως αναφέρει η Allergan, «παρόλο που διαφωνεί [η εταιρεία] με το αίτημα της ANSM, η εταιρεία συνεργάζεται πλήρως με την Αρχή». Η εταιρεία υποστηρίζει στην ανακοίνωσή της πως η αναλογία οφέλους/κινδύνου κατά τη χρήση των συγκεκριμένων προϊόντων παραμένει θετική, συμπληρώνοντας πως «το αίτημα της ANSM δεν βασίζεται σε κανένα νέο επιστημονικό στοιχείο που να αφορά τα εν λόγω προϊόντα», καθώς και πως η γαλλική ρυθμιστική αρχή δεν εντόπισε κανέναν άμεσο κίνδυνο για την υγεία των γυναικών με ενθέματα στήθους τραχείας επιφάνειας.
Σημειώνεται τέλος πως η απώλεια της σήμανσης CE για τα συγκεκριμένα προϊόντα της Allergan δεν επηρεάζει τα υπόλοιπα προϊόντα της εταιρείας, ενώ άλλες εταιρείες που κατασκευάζουν ενθέματα στήθους τραχείας επιφάνειας δεν έχασαν την επίμαχη σήμανση.
Via : www.thepressproject.gr



